Con il continuo sviluppo della tecnologia della biologia molecolare, la relazione tra mutazioni genetiche e difetti e malattie ha acquisito una comprensione sempre più approfondita.Gli acidi nucleici hanno attirato molta attenzione a causa del loro grande potenziale di applicazione nella diagnosi e nel trattamento delle malattie.I farmaci dell'acido nucleico si riferiscono a frammenti di DNA o RNA sintetizzati artificialmente con funzioni di trattamento della malattia.Tali farmaci possono agire direttamente sui geni bersaglio che causano malattie o sugli mRNA bersaglio che causano malattie e svolgere un ruolo nel trattamento delle malattie a livello genico.Rispetto ai tradizionali farmaci a piccole molecole e ai farmaci anticorpali, i farmaci a base di acido nucleico possono regolare l'espressione dei geni che causano malattie dalla radice e hanno le caratteristiche di "trattare i sintomi e curare la causa principale".I farmaci a base di acido nucleico presentano anche evidenti vantaggi come alta efficienza, bassa tossicità e alta specificità.Dal lancio del primo farmaco a base di acido nucleico fomivirsen sodico nel 1998, molti farmaci a base di acido nucleico sono stati approvati per il trattamento clinico.
I farmaci a base di acido nucleico attualmente sul mercato a livello globale includono principalmente acido nucleico antisenso (ASO), piccolo RNA interferente (siRNA) e aptameri di acido nucleico.Ad eccezione degli aptameri dell'acido nucleico (che possono superare i 30 nucleotidi), i farmaci dell'acido nucleico sono generalmente oligonucleotidi composti da 12 a 30 nucleotidi, noti anche come farmaci oligonucleotidici.Inoltre, anche i miRNA, i ribozimi e i deossiribozimi hanno mostrato un grande valore di sviluppo nel trattamento di varie malattie.I farmaci a base di acido nucleico sono diventati oggi uno dei campi più promettenti nella ricerca e nello sviluppo della biomedicina.
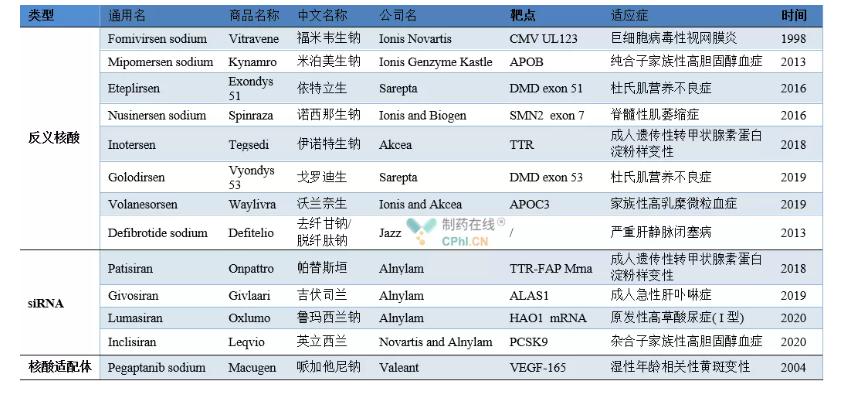
Esempi di farmaci a base di acido nucleico approvati
Acido nucleico antisenso
La tecnologia antisenso è una nuova tecnologia di sviluppo di farmaci basata sul principio della complementazione di base Watson-Crick, utilizzando specifici frammenti complementari di DNA o RNA sintetizzati artificialmente o sintetizzati dall'organismo per regolare in modo specifico l'espressione dei geni bersaglio.L'acido nucleico antisenso ha una sequenza di basi complementare all'RNA bersaglio e può legarsi specificamente ad esso.Gli acidi nucleici antisenso includono generalmente DNA antisenso, RNA antisenso e ribozimi.Tra questi, a causa delle caratteristiche di elevata stabilità e basso costo del DNA antisenso, il DNA antisenso occupa una posizione dominante nell'attuale ricerca e applicazione dei farmaci antisenso dell'acido nucleico.
Fomivirsen sodico (nome commerciale Vitravene) è stato sviluppato da Ionis Novartis.Nell'agosto 1998, la FDA lo ha approvato per il trattamento della retinite da citomegalovirus nei pazienti immunocompromessi (principalmente malati di AIDS), diventando il primo farmaco a base di acido nucleico ad essere commercializzato.Il fomivirsen inibisce l'espressione proteica parziale del CMV legandosi a specifici mRNA (IE2), regolando così l'espressione dei geni virali per ottenere effetti terapeutici.Tuttavia, a causa dell'emergere della terapia antiretrovirale ad alta efficacia, che ha notevolmente ridotto il numero di pazienti, nel 2002 e nel 2006 Novartis ha annullato l'autorizzazione all'immissione in commercio dei farmaci Fomivirsen rispettivamente in Europa e negli Stati Uniti e il prodotto è stato sospeso dal mercato.
Mipomersen sodico (nome commerciale Kynamro) è un farmaco ASO sviluppato dalla società francese Genzyme.Nel gennaio 2013, la FDA lo ha approvato per il trattamento dell'ipercolesterolemia familiare omozigote.Mipomersen inibisce l'espressione della proteina ApoB-100 (apolipoproteina) legandosi all'ApoB-100mRNA, riducendo così in modo significativo il colesterolo umano delle lipoproteine a bassa densità, le lipoproteine a bassa densità e altri indicatori, ma a causa di effetti collaterali come la tossicità epatica, 13 dicembre 2012 Lo stesso giorno, l'EMA ha anche respinto la domanda di licenza di vendita per il farmaco.
Nel settembre 2016, Eteplirsen (nome commerciale Exon 51) sviluppato da Sarepta per il trattamento della distrofia muscolare di Duchenne (DMD) è stato approvato dalla FDA.I pazienti con DMD non possono normalmente esprimere la proteina anti-atrofica funzionale a causa delle mutazioni nel gene DMD nel corpo.Eteplirsen si lega specificamente all'esone 51 dell'RNA pre-messaggero (Pre-mRNA) della proteina, rimuove l'esone 51 e ripristina alcuni geni a valle La normale espressione, trascrizione e traduzione per ottenere parte della distrofina, in modo da ottenere l'effetto terapeutico.
Nusinersen è un farmaco ASO sviluppato da Spinraza per il trattamento dell'atrofia muscolare spinale ed è stato approvato dalla FDA il 23 dicembre 2016. Nel 2018, Inotesen sviluppato da Tegsedi per il trattamento dell'amiloidosi ereditaria da transtiretina dell'adulto è stato approvato dalla FDA.Nel 2019, Golodirsen, sviluppato da Sarepta per il trattamento della distrofia muscolare di Duchenne, è stato approvato dalla FDA.Ha lo stesso meccanismo d'azione di Eteplirsen e il suo sito d'azione diventa l'esone 53. Nello stesso anno, Volanesorsen, sviluppato congiuntamente da Ionis e Akcea per il trattamento dell'iperchilomicronemia familiare, è stato approvato dall'Agenzia europea per i medicinali (EMA).Volanesorsen regola il metabolismo dei trigliceridi inibendo la produzione dell'apolipoproteina C-Ⅲ, ma ha anche l'effetto collaterale di abbassare i livelli piastrinici.
Defibrotide è una miscela di oligonucleotidi con proprietà di plasmina sviluppata da Jazz.Contiene il 90% di DNA a singolo filamento e il 10% di DNA a doppio filamento.È stato approvato dall'EMA nel 2013 e successivamente approvato dalla FDA per il trattamento delle vene epatiche gravi.Malattia occlusiva.Il defibrotide può aumentare l'attività della plasmina, aumentare l'attivatore del plasminogeno, promuovere l'up-regulation della trombomodulina e ridurre l'espressione del fattore di von Willebrand e degli inibitori dell'attivatore del plasminogeno per ottenere effetti terapeutici
siRNA
siRNA è un piccolo frammento di RNA con una lunghezza e una sequenza specifiche prodotte tagliando l'RNA bersaglio.Questi siRNA possono indurre specificamente la degradazione dell'mRNA bersaglio e ottenere effetti di silenziamento genico.Rispetto ai farmaci chimici a piccole molecole, l'effetto di silenziamento genico dei farmaci siRNA ha un'elevata specificità ed efficienza.
L'11 agosto 2018, il primo farmaco siRNA patisiran (nome commerciale Onpattro) è stato approvato dalla FDA e lanciato ufficialmente.Questa è una delle principali pietre miliari nella storia dello sviluppo della tecnologia di interferenza dell'RNA.Patisiran è stato sviluppato congiuntamente da Alnylam e Genzyme, una sussidiaria di Sanofi.È un farmaco siRNA per il trattamento dell'amiloidosi ereditaria mediata dalla tiroxina.Nel 2019, givosiran (nome commerciale Givlaari) è stato approvato dalla FDA come secondo farmaco siRNA per il trattamento della porfiria epatica acuta negli adulti.Nel 2020, Alnylam ha sviluppato un farmaco primario di tipo I per il trattamento di bambini e adulti.Lumasiran con alta ossaluria è stato approvato dalla FDA.Nel dicembre 2020 Inclisiran, sviluppato congiuntamente da Novartis e Alnylam per il trattamento dell'ipercolesterolemia o della dislipidemia mista negli adulti, è stato approvato dall'EMA.
Aptamero
Gli aptameri dell'acido nucleico sono oligonucleotidi che possono legarsi a una varietà di molecole bersaglio come piccole molecole organiche, DNA, RNA, polipeptidi o proteine con elevata affinità e specificità.Rispetto agli anticorpi, gli aptameri dell'acido nucleico hanno le caratteristiche di sintesi semplice, costo inferiore e ampia gamma di bersagli e hanno un potenziale più ampio per l'applicazione di farmaci nella diagnosi, nel trattamento e nella prevenzione delle malattie.
Pegaptanib è il primo farmaco aptamero di acido nucleico sviluppato da Valeant per il trattamento della degenerazione maculare senile umida ed è stato approvato dalla FDA nel 2004. Successivamente, è stato approvato da EMA e PMDA nel gennaio 2006 e nel luglio 2008 ed è stato immesso sul mercato.Pegaptanib inibisce l'angiogenesi attraverso la combinazione di struttura spaziale e fattore di crescita dell'endotelio vascolare per ottenere effetti terapeutici.Da allora, ha incontrato la concorrenza di farmaci simili Lucentis e la sua quota di mercato è diminuita notevolmente.
I farmaci a base di acido nucleico sono diventati un punto caldo nel mercato dei farmaci clinici e dei nuovi farmaci grazie al loro notevole effetto curativo e al breve ciclo di sviluppo.In quanto droga emergente, affronta sfide mentre affronta opportunità.A causa delle sue caratteristiche esogene, la specificità, la stabilità e la consegna efficace degli acidi nucleici sono diventati i criteri principali per giudicare se gli oligonucleotidi possono diventare farmaci a base di acido nucleico altamente efficaci.Gli effetti fuori bersaglio sono sempre stati un punto chiave dei farmaci a base di acido nucleico che non possono essere ignorati.Tuttavia, i farmaci dell'acido nucleico possono influenzare l'espressione dei geni che causano la malattia dalla radice e possono raggiungere la specificità della sequenza a livello di singola base, che ha le caratteristiche di "trattare la causa principale e trattare i sintomi".In considerazione della variabilità di un numero sempre maggiore di malattie, solo il trattamento genetico può ottenere risultati permanenti.Con il continuo miglioramento, perfezionamento e progresso delle tecnologie correlate, i farmaci dell'acido nucleico rappresentati da acidi nucleici antisenso, siRNA e aptameri dell'acido nucleico daranno sicuramente il via a una nuova ondata nel trattamento delle malattie e nell'industria farmaceutica.
Rriferimenti:
[1] Liu Shaojin, Feng Xuejiao, Wang Junshu, Xiao Zhengqiang, Cheng Pingsheng.Analisi di mercato dei farmaci a base di acido nucleico nel mio paese e contromisure[J].Rivista cinese di ingegneria biologica, 2021, 41(07): 99-109.
[2] Chen Wenfei, Wu Fuhua, Zhang Zhirong, Sun Xun.Progressi della ricerca in farmacologia dei farmaci a base di acido nucleico commercializzati[J].Rivista cinese di prodotti farmaceutici, 2020, 51(12): 1487-1496.
[3] Wang Jun, Wang Lan, Lu Jiazhen, Huang Zhen.Analisi dell'efficacia e avanzamento della ricerca dei farmaci a base di acido nucleico commercializzati[J].Giornale cinese delle nuove droghe, 2019, 28(18): 2217-2224.
Informazioni sull'autore: Sha Luo, un addetto alla ricerca e allo sviluppo della medicina cinese, attualmente lavora per una grande azienda nazionale di ricerca e sviluppo di farmaci ed è impegnato nella ricerca e nello sviluppo di nuovi farmaci cinesi.
Prodotti correlati:
Tempo di pubblicazione: 19-nov-2021